| 名称及び製剤 |
治療に関する項目 |
使用上の注意に関する項目 |
作用機序と体内動態 |
化学構造及び物性 |
アセタゾラミド |
〔効〕〔用〕(1)緑内障:(内)(注)1日250〜1000mgを分服,静注・筋注.
(2)てんかん:(内)(注)1日250〜750mgを分服,静注・筋注. (3)肺気腫時の呼吸性アシドーシス:(内)(注)1日1回250〜500mgを内服,静注・筋注.
(4)心性浮腫・肝性浮腫:(内)1日1回250〜500mgを内服. (5)月経前緊張症:(内)1日1回125〜375mgを月経前症状発現時から内服.
(6)メニエール病・メニエール症候群:(内)(注)1日1回250〜750mgを内服,静注・筋注. (7)睡眠時無呼吸症候群:(内)(錠)1日250〜500mgを分服.
|
〔禁〕スルホンアミド系薬剤過敏歴,無尿,急性腎不全,高Cl血症性アシドーシス,体液中Na・K低下,副腎機能不全・アジソン病,慢性閉塞隅角緑内障(長期投与しない).
〔慎〕進行した肝硬変,高齢者,重篤な冠硬化症・脳動脈硬化症,重篤な腎障害,肝疾患・肝障害,重篤な高炭酸ガス血症,ジギタリス剤・糖質副腎皮質ホルモン剤・ACTH投与中,減塩療法時,乳児.
〔相〕(1)他の降圧薬で降圧作用増強. (2)ジギタリスの作用増強.
(3)糖質副腎皮質ホルモン剤・ACTHで過剰のK放出. (4)塩化アンモニウムで利尿効果阻害. (5)大量のビタミンCで腎・尿路結石.
(6)フェノバルビタール,フェニトインでくる病・骨軟化症. (7)アスピリンの大量投与で本剤の副作用増強.
〔副〕〔重大な副作用〕ショック,再生不良性貧血,溶血性貧血,無顆粒球症,皮膚粘膜眼症候群,中毒性表皮壊死症,急性腎不全,腎・尿路結石,精神錯乱.
〔その他の副作用〕電解質失調,発疹,食欲不振,悪心・嘔吐,下痢,腹痛,便秘.(内)四肢の知覚異常,眩暈,頭痛,興奮,いらいら感,うつ状態,傾眠,見当識障害,一過性近視,倦怠感,発熱.
〔妊〕投与しないことが望ましい.
〔貯〕(末)遮光.
〔服薬指導〕夜間の排尿を避けるため,午前中に投与することが望ましい.多量のビタミンCと併用すると腎・尿路結石が起きやすい.
|
〔作用機序〕
(1)緑内障:毛様体上皮中に存在する炭酸脱水酵素の作用を抑制することによって房水の産生を減じ,眼圧を低下.
(2)てんかん:中枢神経組織内に存在する炭酸脱水酵素を抑制し,脳のCO2濃度を局所的に増大させることにより,脳の異常な興奮を抑制して,精神神経系の諸症状を緩解.
(3)呼吸性アシドーシス:炭酸脱水酵素の抑制により,肺胞中のHCO3-の尿中排泄増加.他方代謝性アシドーシスを起こし,H+を増加.増加したH+により呼吸中枢が刺激され,換気量増大,併せて低酸素・炭酸ガス換気応答が改善.
(4)浮腫:腎上皮で炭酸脱水酵素を抑制し,Na+,HCO3-の尿細管再吸収抑制し,利尿効果.
〔体内動態〕
Cmax:20〜30μg/mL,
Tmax:2〜4hr(5mg/kg p.o.)
t1/2:約10〜12hr
尿中排泄率:24時間以内にほとんどが排泄される.
|
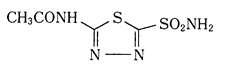
<経口>
mw:222.25
mp:約255℃(分解)
pKa:7.4
★白色〜微黄色の結晶性粉末,においはなく,わずかに苦い.
★極めて溶けにくい.
<注射>
Na塩はmw:244.23(Na塩)
★白色の結晶性粉末で,においはない.
★溶けやすい.
|
|
acetazolamide
 ダイアモックス ダイアモックス
Diamox
(レダリー,武田)
―末
―錠:250mg
―注:500mg
(注射用蒸留水に100mg/mLで溶解した時)
pH:9.0〜10.0
浸透圧比(生理食塩液対比):約3
アセタゾールアミド, アテネゾール, アセタモックス,
ドンモックス, ベタウレール.
|
| アゾセミド |
〔効〕心性浮腫(うっ血性心不全),腎性浮腫,肝性浮腫.
〔用〕(内)1日1回60mgを分服.
|
〔禁〕肝性昏睡,体液中Na・Kの減少.無尿,スルホンアミド誘導体に対して過敏症の既往歴.
〔慎〕進行した肝硬変,肝疾患,肝機能障害,心疾患のある高齢者,重篤な冠硬化症・脳動脈硬化症,重篤な腎障害,本人・血族に痛風・糖尿病,下痢・嘔吐,セファロスポリン系・アミノグリコシド系抗生物質,サリチル酸誘導体又は非ステロイド性消炎鎮痛剤,ジギタリス・糖質副腎皮質ホルモン剤・ACTH投与中,減塩療法時,乳児,高齢者.
〔相〕併用禁忌:(1)昇圧アミン(ノルエピネフリン等)(症圧アミンに対する血管壁の反応性を低下させる).
(2)ツボクラリン及びその類似作用物質(ツボクラリンの麻痺作用を増強). 併用注意:(1)他の降圧剤で降圧作用増強. (2)アミノ糖系抗生物質の聴力障害を増強.
(3)セファロチン,セファロリジンの腎毒性を増強. (4)ジギタリスの作用を増強. (5)糖質副腎皮質ホルモン剤・ACTHで過剰のK放出.
(6)糖尿病用薬の作用を減弱. (7)リチウム(リチウムの再吸収を促進). (8)サリチル酸誘導体(腎の排泄部位にて競合し,毒性増加).
(9)非ステロイド性消炎鎮痛薬(利尿作用の減弱). (10)痛風治療薬(尿酸排泄作用の減弱).
〔副〕電解質失調(低K血症,低Na血症,低Cl性アルカローシス),高尿酸血症,血清クレアチニンの上昇,発疹,肝障害,食欲不振,悪心・嘔吐,胃部不快感,下痢,口渇,眩暈,関節痛.
〔乳〕授乳中止.
〔服薬指導〕夜間の排尿を避けるため,午前中に投与することが望ましい.
|
〔作用機序〕
ヘンレ係蹄の上行脚でNa+,K+-ATPaseの抑制によりNa+及び水の排泄を促進する.
〔体内動態〕
Cmax:235ng/mL,
Tmax:3.0hr(40mg p.o.)
t1/2:2.6〜3.3hr
血漿たん白結合率:97%以上
治療域血漿中濃度:約20ng/mL(推定)
尿中排泄率:4.4%(60mg p.o., 48hr)
主な代謝物:酸化的脱テニル化体, アゾセミドのグルクロン酸抱合体
|
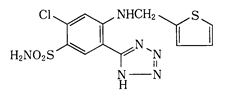
mw:370.83
mp:約226℃(分解)
★白色〜黄白色の結晶性の粉末.無臭,苦い.
★ほとんど溶けない.
油水分配係数:pH4.0以下でn-オクタノール層に,pH12.9以上では水層にそれぞれ99%以上分配される.
|
|
azosemide
 ダイアート ダイアート
Diart
(三和化学)
―錠:30mg, 60mg
|
| インダパミド |
〔効〕本態性高血圧症.
〔用〕(内)1日1回2mg.朝食後服用.
|
〔禁〕無尿,急性腎不全,体液中のNa・Kの減少,チアジド系薬過敏歴.
〔慎〕進行した肝硬変症,心疾患のある高齢者,重篤な冠硬化症・脳動脈硬化症,重篤な腎障害,肝疾患・肝障害,本人・血族に痛風・糖尿病,下痢・嘔吐中,高Ca血症・副甲状腺機能亢進症,ジギタリス剤・糖質副腎皮質ホルモン剤・ACTHの投与中,減塩療法時,乳児,交感神経切除後,高齢者.
〔相〕併用注意:(1)バルビツール酸誘導体,アヘンアルカロイド系麻薬で起立性低血圧が増強.
(2)アルコールで起立性低血圧が増強. (3)ノルエピネフリン等の昇圧アミンの併用で昇圧アミンに対する血管壁の反応性を低下. (4)ツボクラリン及びその類似作用物質の併用でその麻酔作用が増強.
(5)糖質副腎皮質ホルモン剤,ACTHの併用で過剰のカリウム放出. (6)リチウムの毒性を増強.. (7)糖尿病薬の作用を減弱.
〔副〕血小板減少,白血球減少,肝障害,低Na血症,低K血症,低Cl性アルカローシス,血中Caの上昇,尿素窒素・クレアチニン・総コレステロールの上昇,高尿酸血症,高血糖症,発疹,顔面潮紅,光線過敏症,食欲不振,悪心・嘔吐,口渇,便秘,胃部不快感,胃重感,眩暈,頭痛・頭重,眠気,いらいら感.
〔乳〕授乳中止.
|
〔作用機序〕
遠位尿細管におけるNa+,Cl-の再吸収を抑制して水の排泄を増加させる.
〔体内動態〕
Cmax:84ng/mL,
Tmax:約2hr(2mg p.o.)
t1/2:7.5〜10.4hr
血漿たん白結合率:約83%
尿中排泄率:49.5%
|
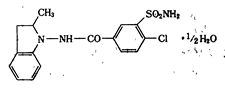
mw:374.85
mp:167.5〜170.5℃
★白色の結晶性の粉末.においはなく,味ははじめなく,後に苦い.
pKa:9.2
★ほとんど溶けない.
油水分配係数:25.2(n-オクタノール/pH7.0)
|
|
indapamide
 ナトリックス ナトリックス
Natrix
(京都薬品,住友,日本セルヴィエ)
―錠:1mg, 2mg
テナキシル, ナシンドレン.
|
フロセミド |
〔効〕高血圧症(本態性,腎性など),悪性高血圧,心性浮腫(うっ血性心不全),腎性浮腫,肝性浮腫,尿路結石排出促進.(内)のみ月経前緊張症,末梢血管障害による浮腫,(注)のみ脳浮腫.100mg注は急性・慢性腎不全による乏尿.
〔用〕(内)1日1回40〜80mgを毎日又は隔日服用. (注)1日1回20mgを静注・筋注.
腎機能不全時:250mgを1時間以上で点滴静注,利尿反応がなければ漸増,投与速度は4mg/分以下
|
〔禁〕無尿,肝性昏睡,体液中Na・K減少,スルフォンアミド誘導体過敏症.テルフェナジン又はアステミゾール投与中(100mg注),腎毒性・肝毒性物質による中毒からの腎不全,肝性昏睡を伴う腎不全,著しい循環血液量の減少・血圧低下.
〔慎〕進行した肝硬変症,重篤な冠硬化症・脳動脈硬化症・腎障害,高齢者,肝疾患・肝機能障害,痛風・糖尿病の家族歴,下痢・嘔吐中,ジギタリス剤・糖質副腎皮質ホルモン剤・ACTH又はグリチルリチン製剤投与中,減塩療法時,乳児,未熟児.
〔相〕併用注意:(1)昇圧アミンに対する血管壁の反応性を低下.
(2)ツボクラリン類の麻痺作用を増強. (3)他の降圧薬の作用増強. (4)アミノ糖系抗生物質の聴力障害増強. (5)セフェム系およびアミノ糖系抗生物質の腎毒性を増強.
(6)ジギタリス剤の作用増強. (7)糖質副腎皮質ホルモン剤・ACTH及びグリチルリチン製剤で過剰のK放出. (8)糖尿病用薬の作用減弱.
(9)リチウムの毒性増強. (10)サリチル酸誘導体の毒性発現. (11)非ステロイド性消炎鎮痛薬で本剤の作用減弱. (12)痛風治療剤の作用減弱.
(13)(注)シスプラチンの聴力障害増強. (14)カルバマゼピンで症候性低Na血症.
〔副〕〔重大な副作用〕ショック・アナフィラキシー様症状,再生不良性貧血,汎血球減少症,無顆粒球症,赤芽球癆,水疱性類天疱瘡,難聴.皮膚粘膜眼症候群,心室性不整脈.
〔その他の副作用〕貧血,顆粒球減少,白血球減少,血小板減少,低Na・K血症,低Cl性アルカローシス,高尿酸血症,高血糖症,発疹,蕁麻疹,発赤,光線過敏症,食欲不振,悪心・嘔吐,下痢,口渇,膵炎,肝障害,腎障害,眩暈,頭痛,知覚異常,脱力感,倦怠感,起立性低血圧,筋けいれん.
〔乳〕授乳を避ける.
〔小児〕未熟児で腎石灰化症.乳児で電解質バランスがくずれやすい.
〔服薬指導〕本剤の保管は直射日光を避け,できるだけ遮光性のある容器などに保存する.
夜間の排尿を避けるため,午前中に投与することが望ましい.
降圧作用→自動車の運転など注意.
|
〔作用機序〕
ヘンレ係蹄の上行脚でNa+,K+-ATPase抑制によりNa+及び水の排泄を促進する.
〔体内動態〕
Cmax:1μg/mL,
Tmax:2hr(40mg p.o.)
F:61%
Vd:0.11L/kg
CL:2.0mL/min/kg
t1/2:30〜100min(p.o.)
血漿たん白結合率:97.4〜97.6%
尿中排泄率:88%(i.v.)
主な代謝物:4-chloro-5-sulfamoyl-anthranilic acid
|
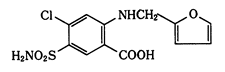
mw:330.75
mp:約205℃(分解)
★白色の結晶又は結晶性粉末.においはない.
pKa:3.9
★ほとんど溶けない.
|
|
furosemide
 ラシックス ラシックス
Lasix
(ヘキスト)
―細粒:1g中40mg
―錠:20mg, 40mg
―注:2mL中20mg, 10mL中100mg
pH:8.6〜9.6
浸透圧比(生理食塩液対比):約1
|
 オイテンシン オイテンシン
Eutensin
(ヘキスト)
―徐放性カプセル:40mg
<構造> マルチプルユニット型, 腸溶性カプセル製剤 |
〔効〕本態性高血圧症
〔用〕(内)1日40〜80mgを1〜2回に分服.
|
| メトラゾン |
〔効〕〔用〕(内)本態性高血圧症:1日1回2.5mgを朝服用.心性浮腫・腎性浮腫・肝性浮腫:1日5mgを朝服用.
|
〔禁〕無尿,急性腎不全,体液中のナトリウム・カリウム減少,本剤又は,チアジド系薬剤並びにその類似化合物(例えばクロルタリドン等のスルホンアミド誘導体)に過敏症の既往歴,テルフェナジン又はアステミゾールを投与中.
〔慎〕進行した肝硬変症,重篤な冠硬化症又は脳動脈硬化症,重篤な腎障害,肝疾患・肝機能障害,本人又は両親,兄弟に痛風,糖尿病の患者,下痢,嘔吐,高カルシウム血症,副甲状腺機能亢進症,ジギタリス剤,糖質副腎皮質ホルモン剤又はACTHの投与中,減塩療法時,高齢者,乳児,交感神経切除後.
〔相〕(1)バルビツール酸系薬,アヘンアルカロイド系麻薬,飲酒により起立性低血圧の増強.
(2)昇圧アミンに対する血管壁の反応性低下,ツボクラリン類の麻痺作用を増強. (3)他の降圧薬で作用増強. (4)ジギタリスの作用増強.
(5)糖質副腎皮質ホルモン・ACTHで過剰のK放出. (6)糖尿病用薬の作用を減弱. (7)乳酸ナトリウムで本剤の代謝性アルカローシス,低カリウム血症を増強.
(8)リチウム製剤の毒性を増強. (9)グリチルリチン製剤で血清カリウム値の低下. (10)インドメタシン等で本剤の作用減弱. (11)スルフィンピラゾンの尿酸排泄作用に拮抗.
(12)クエン酸トレミフェンで血中カルシウム上昇の危険性.
〔副〕低Na血症・低K血症,低Cl性アルカローシス,高尿酸血症,高血糖症,高コレステロール血症,光線過敏症,発疹,蕁麻疹,低血圧,起立性低血圧,胸部不快感,動悸,腎障害,食欲不振,口渇,悪心・嘔吐,胃部不快感,胃腸障害,便秘,下痢,眩暈・ふらつき,頭痛・頭重感,手足のしびれ,肝障害,脱力・倦怠感,不快感,筋肉のつれ,白血球減少.
〔乳〕授乳中止.
〔服薬指導〕夜間の排尿を避けるため,午前中に投与することが望ましい.
|
〔作用機序〕
遠位尿細管におけるNa+,Cl-の再吸収を抑制して水の排泄を増加させる.
〔体内動態〕
Cmax:約121.8ng/mL,
Tmax:約6hr(20mg p.o.)
t1/2:3.74hr
血漿たん白結合率:約95%
尿中排泄率:13〜33%(20mg p.o., 48hr)
|
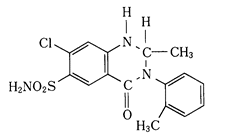
mw:365.84
mp:252〜264℃(分解)
★白色〜微黄白色の結晶又は結晶性粉末.においはない.
★ほとんど溶けない.
|
metolazone
 ノルメラン ノルメラン
Normelan
(ノバルティス)
―錠:2.5mg |
| カルペリチド(遺伝子組換え) |
〔効〕急性心不全(慢性心不全の急性増悪期を含む).
〔用〕(注)1分間当たり0.1μg/kgを持続静脈内投与する.病態に応じて1分間当たり0.2μg/kgまで増量できる.
|
〔禁〕重篤な低血圧,又は心原性ショック,右室梗塞,脱水症状.
〔慎〕低血圧,右房圧が正常域にある患者,利尿剤との併用,脱水傾向,ネフローゼ症候群,ヘマトクリット値の著しい高値,重篤な肝障害,腎障害.
〔副〕〔重大な副作用〕血圧低下,低血圧性ショック,徐脈→減量又は中止.
〔その他の副作用〕顔のほてり,洞性頻脈など.
〔高齢〕過量投与にならないように注意する.
〔妊〕有益性が危険性を上回る場合のみ投与する.
〔乳〕授乳を避ける.
〔小児〕安全性は確立していない.
〔備〕他の注射剤と混合せずに用いることが望ましい,過量投与→中止.血圧などの回復が不十分な場合あるいは徐脈を伴う場合には,輸液,硫酸アトロピンの静注.
|
〔作用機序〕
α型ヒト心房性ナトリウム利尿ペプチド受容体に結合し,膜結合型グアニル酸シクラーゼを活性化させて細胞内cGMPを増加させ,動脈血管の拡張(後負荷の軽減)と静脈血管の拡張ならびに尿量増加(前負荷の軽減)を示す.
〔体内動態〕
Css:1.6ng/mL(0.1μg/kg/minで60分間持続点滴時),
t1/2α:4.2min
t1/2β:28.8min
Vc:478mL/kg
Vss:589mL/kg
CL:65mL/min/kg
尿中排泄率:0.2μg/kg/minで持続点滴時投与量の0.001%
|
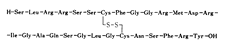
★白色の粉末ないし塊で,酢酸臭.
[α]20D:-55〜-65°(水)
★溶けやすい.
|
|
carperitide (genetical recombination)
 ハンプ ハンプ
Hanp
(ゼリア新薬,サントリー)
―注 :1000μg :1000μg
浸透圧比(生理食塩液対比):約1
◆使用上の注意改定指示
H13/03/26
H14/08/12
|
